- Uretroplastica peniena 1° tempo sec. Johanson
- Uretroplastica peniena 1° tempo con innesto dorsale (sec. Asopa) di mucosa buccale
- Uretroplastica peniena 1° tempo con innesto dorsale (sec. Asopa) di prepuzio
- Uretroplastica peniena 1° tempo con innesto dorsale (sec. Bracka) di mucosa buccale
- Uretroplastica peniena 1° tempo con innesto dorsale (sec. Bracka) di prepuzio
- Uretroplastica peniena 2° tempo
- Uretroplastica peniena in tempo unico con innesto dorsale (sec. Asopa) di mucosa buccale
- Uretroplastica peniena in tempo unico con innesto dorsale (sec. Asopa) di prepuzio
Uretroplastica peniena 1° tempo sec. Johanson
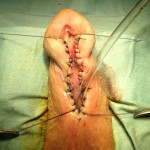
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Si confeziona uretrostomia medio-peniena ed i margini dell’uretra aperta vengono suturati alla cute peniena (sec. Johanson) [foto Pen1, Pen2, Pen3, Pen4]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato).



TEMPO DI ESECUZIONE: Circa 30 min-1h
TERAPIA: Chinolonici per 5 giorni.
GESTIONE PAZIENTE: Il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene. Dimissioni in 2° giornata postoperatoria senza catetere.
MEDICAZIONI: Medicare con Betadine soluzione, ma già a 5 giorni dall’intervento chirurgico si può utilizzare acqua o soluzione fisiologica, fino alla guarigione della ferita (cioè fino a quando la ferita risulta asciutta). Ghiaccio sul pene per 3-4 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta molto compromesso. Questo intervento permette al paziente di riprendere ad urinare da subito e senza difficoltà. Successivamente, a distanza di mesi, si stabiliranno le altre tappe ricostruttive. Può essere indicata nei casi complessi di lichen sclerosus dell’uretra e dei genitali, nonchè nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine.
COMPLICANZE: sanguinamento, infezione <1%.
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 323 uretroplastiche sec. Johanson, dell’uretra peniena (distale, media, prossimale e totale). Fallimenti 7, Successi 316. Percentuale di successo 97.7%
APPROFONDISCI:
The treatment of urethral stricture by excision.
Russel RH
Br J Surg 1914;2:375 * No abstract available
Reconstruction of the male urethra in strictures.
Johanson B.
Acta Chir Scand 1953: 176:3 * No abstract available
Uretroplastica peniena 1° tempo con innesto dorsale (sec. Asopa) di mucosa buccale
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi . Incisione mediana del piatto uretrale cicatriziale e lateralizzazione del piatto uretrale sclerotico per tutta la lunghezza della stenosi. Asportazione parziale dei tessuti uretrali cicatriziali ed ampliamento del piatto uretrale sec. Asopa con innesto di mucosa buccale (prelevata dalla guancia destra o sinistra) [foto P20, P21]. Effettuare l’esame istologico del tessuto uretrale cicatriziale asportato. I margini dell’uretra peniena aperta vengono suturati ai margini laterali mediante sutura continua. Si confeziona uretrostomia medio-peniena. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato). Connettivina, a copertura del graft, fissata con punti di sutura.


TEMPO DI ESECUZIONE: Circa 1,5h
TERAPIA: Chinolonici per 5 giorni.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene e sulla guancia dove è stato fatto il prelievo di mucosa buccale. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: Le garze di connettivina legate con punti di sutura ed il catetere verranno rimossi in 8 giornata postoperatoria. Ghiaccio sul pene per 3-4 giorni. Rimosse le garze legate con punti di sutura, sarà ben visibile l’innesto, sopra il quale va applicato gel rigenerante. Pulire la ferita con Soluzione Fisiologica o con acqua. Le medicazioni vanno effettuate per circa 20-30 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta non del tutto compromesso, è possibile effettuare un innesto di mucosa buccale. Successivamente, a distanza di mesi, quando il piatto uretrale è stabilizzato [foto P3], si potrà effettuare la chiusura. Questo intervento permette al paziente di riprendere ad urinare da subito e senza difficoltà, ed inoltre abbiamo già preparato il piatto uretrale per la chiusura. Può essere indicata nei casi complessi di lichen sclerosus dell’uretra e dei genitali, nonchè nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Attenzione! Effettuare questo tipo di uretroplastica solo se il piatto uretrale non risulta molto compromesso, diversamente l’intervento esiterebbe in una parziale o completa retrazione cicatriziale dell’innesto.

COMPLICANZE: sanguinamento, infezione <1%. Retrazione cicatriziale dell’innesto 1,5%.
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 65 uretroplastiche peniena 1° tempo sec. Asopa con mucosa buccale. Successi 64, Fallimenti 1. Percentuale di successo 98.5%.
APPROFONDISCI:
Dorsal free graft urethroplasty for urethral stricture by ventral sagittal urethrotomy approach. (Asopa HS, Garg M, Singhal GG, Singh L, Asopa J, Nischal ) Urology. 2001 Nov;58(5):657-9.
Dorsal buccal mucosal graft urethroplasty for anterior urethral stricture by Asopa technique. (Pisapati VL, Paturi S, Bethu S, Jada S, Chilumu R, Devraj R, Reddy B, Sriramoju V.) Eur Urol. 2009 Jul;56(1):201-5. Epub 2008 Jun 9.
Uretroplastica peniena 1° tempo con innesto dorsale (sec. Asopa) di prepuzio
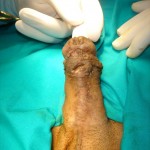
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Incisione mediana del piatto uretrale cicatriziale e lateralizzazione del piatto uretrale sclerotico per tutta la lunghezza della stenosi [foto prep 1, prep2, prep 3, prep 4, prep 5]. Asportazione parziale dei tessuti uretrali cicatriziali ed ampliamento del piatto uretrale sec. Asopa con innesto di prepuzio (prelevato dalla superficie dorsale del pene o dalla superficie laterale del pene o tramite semicirconcisione o circoncisione) [foto prep 5]. Effettuare l’esame istologico del tessuto uretrale cicatriziale asportato. I margini dell’uretra peniena aperta vengono suturati ai margini laterali mediante sutura continua. Si confeziona uretrostomia medio-peniena. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato). Connettivina, a copertura del graft, fissata con punti di sutura.




TEMPO DI ESECUZIONE: Circa 1,5h
TERAPIA: Chinolonici per 5 giorni.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: Le garze di connettivina legate con punti di sutura ed il catetere verranno rimossi in 8 giornata postoperatoria. Ghiaccio sul pene per 3-4 giorni. Rimosse le garze legate con punti di sutura, sarà ben visibile l’innesto, sopra il quale va applicato gel rigenerante. Pulire la ferita con Soluzione Fisiologica o con acqua. Le medicazioni vanno effettuate per circa 20-30 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta non del tutto compromesso, è possibile effettuare un innesto di prepuzio. Successivamente, a distanza di mesi, si stabiliranno le altre tappe ricostruttive. Questo intervento permette al paziente di riprendere ad urinare da subito e senza difficoltà, ed inoltre abbiamo già preparato il piatto uretrale per la chiusura. Può essere indicata nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Controindicata, invece, nei casi di lichen sclerosus dell’uretra e dei genitali. Attenzione! Effettuare questo tipo di uretroplastica solo se il piatto uretrale non risulta molto compromesso, diversamente l’intervento esiterebbe in una parziale o completa retrazione cicatriziale dell’innesto.
COMPLICANZE: sanguinamento, infezione <1%. Retrazione cicatriziale dell’innesto 1,5% (considerata una retrazione cicatriziale comune, non riferita alla casistica di seguito)
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 53 uretroplastiche peniena 1° tempo sec. Asopa con prepuzio. Successi 53, Fallimenti 0. Percentuale di successo 100%
APPROFONDISCI:
Dorsal free graft urethroplasty for urethral stricture by ventral sagittal urethrotomy approach. (Asopa HS, Garg M, Singhal GG, Singh L, Asopa J, Nischal A.) Urology. 2001 Nov;58(5):657-9.
Dorsal buccal mucosal graft urethroplasty for anterior urethral stricture by Asopa technique. (Pisapati VL, Paturi S, Bethu S, Jada S, Chilumu R, Devraj R, Reddy B, Sriramoju V.) Eur Urol. 2009 Jul;56(1):201-5. Epub 2008 Jun 9.
Uretroplastica peniena 1° tempo con innesto dorsale (sec. Bracka) di mucosa buccale
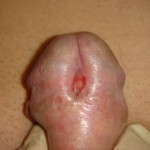
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Ampia asportazione di tutto il piatto uretrale cicatriziale e sua sostituzione con innesto di mucosa buccale (prelievo da guancia destra o sinistra). Effettuare l’esame istologico del tessuto uretrale cicatriziale asportato. I margini dell’uretra peniena aperta vengono suturati ai margini laterali mediante sutura continua. Si confeziona uretrostomia medio-peniena [foto Br20, Br21]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato). Connettivina, a copertura dell’innesto, fissata con punti di sutura.

TEMPO DI ESECUZIONE: Circa 1,5h
TERAPIA: Chinolonici per 5 giorni.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene e sulla guancia dove è stato fatto il prelievo di mucosa buccale. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: Le garze di connettivina legate con punti di sutura ed il catetere verranno rimossi in 8 giornata postoperatoria. Ghiaccio sul pene per 3-4 giorni. Rimosse le garze legate con punti di sutura, sarà ben visibile l’innesto, sopra il quale va applicato gel rigenerante. Pulire la ferita con Soluzione Fisiologica o con acqua. Le medicazioni vanno effettuate per circa 20-30 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta estesamente compromesso, è consigliabile la sua totale rimozione e sostituzione con un innesto di mucosa buccale. Successivamente, a distanza di mesi, si stabiliranno le altre tappe ricostruttive. Questo intervento permette al paziente di riprendere ad urinare da subito e senza difficoltà, ed inoltre abbiamo già preparato il piatto uretrale per la chiusura. Può essere indicata nei casi complessi di lichen sclerosus dell’uretra e dei genitali, nonchè nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Attenzione! Rimuovere interamente tutto il tessuto uretrale cicatriziale.
COMPLICANZE: sanguinamento, infezione <1%. Retrazione cicatriziale dell’innesto 1,5% (considerata una retrazione cicatriziale comune, non riferita alla casistica di seguito)
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 44 uretroplastiche peniena 1° tempo sec. Bracka con mucosa buccale. Successi 42, Fallimenti 2. Percentuale di successo 95.5%
APPROFONDISCI:
The role of two-stage repair in modern hypospadiology.
Bracka A. Indian J Urol. 2008 Apr;24(2):210-8.
Hypospadias surgery: when, what and by whom? (Manzoni G, Bracka A, Palminteri E, Marrocco G.) BJU Int. 2004 Nov;94(8):1188-95.
Initial experience with staged buccal graft (Bracka) hypospadias reoperations. (Snodgrass W, Elmore J.) J Urol. 2004 Oct;172(4 Pt 2):1720-4; discussion 1724.
Uretroplastica peniena 1° tempo con innesto dorsale (sec. Bracka) di prepuzio
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Ampia asportazione di tutto il piatto uretrale cicatriziale e sua sostituzione con innesto di prepuzio (prelevato dalla superficie dorsale del pene o dalla superficie laterale del pene o tramite semicirconcisione o circoncisione). Effettuare l’esame istologico del tessuto uretrale cicatriziale asportato. I margini dell’uretra peniena aperta vengono suturati ai margini laterali con sutura continua. Si confeziona uretrostomia medio-peniena [foto Br23]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato). Connettivina, a copertura dell’innesto, fissata con punti di sutura.

TEMPO DI ESECUZIONE: Circa 1,5h
TERAPIA: Chinolonici per 5 giorni.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: Le garze di connettivina legate con punti di sutura ed il catetere verranno rimossi in 8 giornata postoperatoria. Ghiaccio sul pene per 3-4 giorni. Rimosse le garze legate con punti di sutura, sarà ben visibile l’innesto, sopra il quale va applicato gel rigenerante. Pulire la ferita con Soluzione Fisiologica o con acqua. Le medicazioni vanno effettuate per circa 20-30 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta estesamente compromesso, è consigliabile la sua totale rimozione e sostituzione con con innesto di prepuzio. Successivamente, a distanza di mesi, si stabiliranno le altre tappe ricostruttive. Questo intervento permette al paziente di riprendere ad urinare da subito e senza difficoltà, ed inoltre abbiamo già preparato il piatto uretrale per la chiusura. Può essere indicata nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Controindicata, invece, nei casi di lichen sclerosus dell’uretra e dei genitali. Attenzione! Rimuovere interamente tutto il tessuto uretrale cicatriziale.
COMPLICANZE: sanguinamento, infezione <2%. Retrazione cicatriziale dell’innesto 1,5% (considerata una retrazione cicatriziale comune, non riferita alla casistica di seguito)
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 19 uretroplastiche peniena 1° tempo sec. Bracka con prepuzio. Successi 19, Fallimenti 0. Percentuale di successo 100%
*Attenzione la percentuale di successo al 100% non vuole significare che il prepuzio non causa fallimenti!
APPROFONDISCI:
The role of two-stage repair in modern hypospadiology.
Bracka A.
Indian J Urol. 2008 Apr;24(2):210-8.
Hypospadias surgery: when, what and by whom?
Manzoni G, Bracka A, Palminteri E, Marrocco G.
BJU Int. 2004 Nov;94(8):1188-95.
Initial experience with staged buccal graft (Bracka) hypospadias reoperations.
Snodgrass W, Elmore J.
J Urol. 2004 Oct;172(4 Pt 2):1720-4; discussion 1724.
Uretroplastica peniena 2° tempo
TECNICA : Si scolpisce il piatto uretrale precedentemente ricostruito. Asportazione dei tessuti cicatriziali del pene e dell’uretra, esito dei pregressi interventi. Ricostruzione della neouretra su catetere Nelaton 18 Fr e sua copertura con strati di dartos. Ricostruzione del meato e del glande [FOTO PC1, PC2, PC3]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato) per 14 giorni (sempre collegato al sacchetto della raccolta urine).



TEMPO DI ESECUZIONE: Circa 1h
TERAPIA: Chinolonici per 5 giorni. poi a seguire Monuril 1 bustina ogni 5 giorni, fino alla rimozione del catetere.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: si consiglia di medicare con Betadine soluzione, ma già a 3 giorni dall’intervento chirurgico si può utilizzare acqua o soluzione fisiologica, fino alla guarigione della ferita (cioè fino a quando la ferita risulta asciutta). Ghiaccio sul pene per 3-4 giorni.
COMPLICANZE: sanguinamento, infezione <1%. Fistola uretrale 5%.
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 121 uretroplastiche peniene 2° tempo. Successi 107, Fallimenti 7. Percentuale di successo 88.5%
Uretroplastica peniena in tempo unico con innesto dorsale (sec. Asopa) di mucosa buccale
TECNICA : Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Incisione mediana del piatto uretrale cicatriziale e lateralizzazione del piatto uretrale sclerotico per tutta la lunghezza della stenosi. Asportazione parziale dei tessuti uretrali cicatriziali ed ampliamento uretrale dorsale (sec. Asopa) con innesto di mucosa buccale (prelievo da guancia destra o sinistra). Ricostruzione delle ali del glande e del neo-meato. Tubularizzazione del neopiatto uretrale ampliato su catetere Nelaton 16Fr o 18 Fr. Spongioplastica e copertura dell’uretra con strati di dartos [foto P21, P22, P23]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato) per 14 giorni (sempre collegato al sacchetto della raccolta urine).



TEMPO DI ESECUZIONE: Circa 1,5-2h
TERAPIA: Chinolonici per 5 giorni. poi a seguire Monuril 1 bustina ogni 5 giorni, fino alla rimozione del catetere.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene e sulla guancia dove è stato fatto il prelievo di mucosa buccale. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: si consiglia di medicare con Betadine soluzione, ma già a 7 giorni dall’intervento chirurgico si può utilizzare acqua o soluzione fisiologica, fino alla guarigione della ferita (cioè fino a quando la ferita risulta asciutta). Ghiaccio sul pene per 3-4 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta non del tutto compromesso e se la vascolarizzazione dell’uretra è buona, è possibile effettuare un intervento in tempo unico. Può essere indicata nei casi complessi di lichen sclerosus dell’uretra e dei genitali, nonchè nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Attenzione! evitare questo intervento in caso di piatto uretrale estesamente compromesso o in presenza di deficit della vascolarizzazione dell’uretra peniena.
COMPLICANZE: sanguinamento, infezione <1%. Fistola uretrale 5%.
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 60 uretroplastiche peniena in tempo unico sec. Asopa con mucosa buccale. Successi 53, Fallimenti 7. Percentuale di successo 88.3%
APPROFONDISCI
Dorsal free graft urethroplasty for urethral stricture by ventral sagittal urethrotomy approach. (Asopa HS, Garg M, Singhal GG, Singh L, Asopa J, Nischal A.) Urology. 2001 Nov;58(5):657-9.
Dorsal buccal mucosal graft urethroplasty for anterior urethral stricture by Asopa technique. (Pisapati VL, Paturi S, Bethu S, Jada S, Chilumu R, Devraj R, Reddy B, Sriramoju V.) Eur Urol. 2009 Jul;56(1):201-5. Epub 2008 Jun 9.
Uretroplastica peniena in tempo unico con innesto dorsale (sec. Asopa) di prepuzio
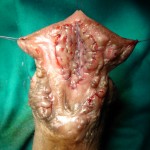
TECNICA: Apertura mediana ventrale dell’uretra, per tutta la lunghezza della stenosi. Incisione mediana del piatto uretrale cicatriziale e lateralizzazione del piatto uretrale sclerotico per tutta la lunghezza della stenosi. Asportazione parziale dei tessuti uretrali cicatriziali ed ampliamento uretrale dorsale (sec. Asopa) con innesto di prepuzio (prelevato dalla superficie dorsale del pene o dalla superficie laterale del pene o tramite semicirconcisione o circoncisione).Ricostruzione delle ali del glande e del neo-meato. Tubularizzazione del neopiatto uretrale ampliato su catetere Nelaton 16Fr o 18 Fr. Spongioplastica e copertura dell’uretra con strati di dartos [foto Prep 5, Prep 6, Prep 7]. Si consiglia Catetere Foley 14 Fr (siliconato e scanalato) per 14 giorni (sempre collegato al sacchetto della raccolta urine).


TEMPO DI ESECUZIONE: Circa 1,5-2h
TERAPIA: Chinolonici per 5 giorni. poi a seguire Monuril 1 bustina ogni 5 giorni, fino alla rimozione del catetere.
GESTIONE PAZIENTE: il paziente si può alzare in 1 giornata postoperatoria. Ghiaccio sul pene. Dimissioni in 2° giornata postoperatoria.
MEDICAZIONI: si consiglia di medicare con Betadine soluzione, ma già a 7 giorni dall’intervento chirurgico si può utilizzare acqua o soluzione fisiologica, fino alla guarigione della ferita (cioè fino a quando la ferita risulta asciutta). Ghiaccio sul pene per 3-4 giorni.
QUANDO IMPIEGARE QUESTO TIPO DI URETROPLASTICA: quando si apre l’uretra, se il piatto uretrale risulta non del tutto compromesso e se la vascolarizzazione dell’uretra è buona, è possibile effettuare un intervento in tempo unico. Può essere indicata nei casi di ipospadia fallita (pazienti plurioperati per ipospadia) e nella ipospadia vergine. Controindicata, invece, nei casi di lichen sclerosus dell’uretra e dei genitali. Attenzione! evitare questo intervento in caso di piatto uretrale mediamente compromesso o in presenza di deficit della vascolarizzazione dell’uretra peniena
COMPLICANZE: sanguinamento, infezione <2%. Fistola uretrale 5%.
PERCENTUALE DI SUCCESSO CENTRO URETRA AREZZO: Casistica Dr. Palminteri aggiornata al 31/12/2011. Effettuate 62 uretroplastiche peniena in tempo unico sec. Asopa con prepuzio. Successi 48, Fallimenti 14. Percentuale di successo 77.5%
APPROFONDISCI
Dorsal free graft urethroplasty for urethral stricture by ventral sagittal urethrotomy approach. (Asopa HS, Garg M, Singhal GG, Singh L, Asopa J, Nischal A.) Urology. 2001 Nov;58(5):657-9.
Dorsal buccal mucosal graft urethroplasty for anterior urethral stricture by Asopa technique. (Pisapati VL, Paturi S, Bethu S, Jada S, Chilumu R, Devraj R, Reddy B, Sriramoju V.) Eur Urol. 2009 Jul;56(1):201-5. Epub 2008 Jun 9.










































































